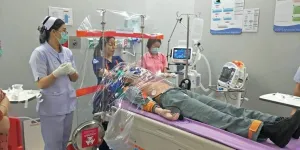
แถลงข่าวร่วม สภาเภสัชกรรม นักวิชาการ ภาคประชาสังคมด้านสาธารณสุข ยกบทเรียนระบบทรัพย์สินทางปัญญาไทย ที่ทำให้สามารถเข้าถึงยาโลพินาเวียร์/ลิโทนาเวียร์ และยาโอเซลทามิเวียร์ สูตรการให้ยาที่สามารถรักษาโคโรน่าไวรัสสายพันธุ์ใหม่ได้ ชี้ ต้องจับตามองเอฟทีเอที่รัฐบาลไทยจะทำ กรมทรัพย์สินทางปัญญาต้องทำงานเรื่องสิทธิบัตรอย่างรอบคอบและเปิดกว้าง
ที่มาภาพประกอบ: Wikipedia
4 ก.พ. 2563 ที่ห้องประชุมสภาเภสัชกรรม ชั้น 10 อาคารที่ทำการสภาวิชาชีพด้านสุขภาพ กระทรวงสาธารณสุข มีการแถลงข่าวร่วม ระหว่างสภาเภสัชกรรม ศูนย์วิชาการเฝ้าระวังและพัฒนาระบบยา (กพย.) มูลนิธิเข้าถึงเอดส์ เครือข่ายผู้ติดเชื้อเอชไอวี/เอดส์ ประเทศไทย เครือข่ายนักวิชาการเพื่อการเข้าถึงยา และกลุ่มศึกษาข้อตกลงเขตการค้าเสรีภาคประชาชน (FTA Watch) ในหัวข้อ "LPV/r และ Oseltamivir ยารักษาโคโรน่าไวรัสสายพันธุ์ใหม่: กรณีศึกษาพัฒนาคุณภาพระบบทรัพย์สินทางปัญญาเพื่อการเข้าถึงยา" โดยมีใจความดังนี้
บทเรียนระบบทรัพย์สินทางปัญญาเพื่อการเข้าถึงยาที่ทำให้ประเทศไทยสามารถใช้ยาโลพินาเวียร์/ลิโทนาเวียร์ (lopinavir/ritonavir (LPV/r)) และยาโอเซลทามิเวียร์ (Oseltamivir) เป็นยารักษาโคโรน่าไวรัสสายพันธุ์ใหม่ในราคาที่ระบบประกันสุขภาพสามารถรองรับได้ ในขณะที่ยา LPV/r บางตำรับยังติดสิทธิบัตรในสหรัฐอเมริกาและอีกหลายประเทศ ทำให้ยามีราคาแพงและยากต่อการเข้าถึง
ข้อมูลด้านทรัพย์สินทางปัญญาที่เกี่ยวข้องกับยาโลพินาเวียร์/ริโทนาเวียร์)
และยาโอเซลทามิเวียร์
1. LPV/r เป็นยาสูตรผสมรวมเม็ดของยาโลพินาเวียร์และยาริโทนาเวียร์ (Lopinavir/Ritonavir) ที่ประเทศไทยได้ประกาศบังคับใช้สิทธิเพื่อนำเข้าหรือผลิตยาโดยรัฐ หรือที่เรียกว่า CL (Compulsory Licensing) ตั้งแต่ปี 2550 ซึ่งเป็นยาสูตรสำรองที่สองสำหรับรักษาเอชไอวี จากมาตราการ CL ดังกล่าวทำให้ไทยมียาคุณภาพในราคาที่ไม่แพงใช้อย่างต่อเนื่อง
ในช่วงแรกหลังประกาศใช้มาตรการ CL ไทยนำเข้ายานี้จากอินเดีย ในปัจจุบันองค์การเภสัชกรรมสามารถผลิตเองได้ จึงยิ่งทำให้ราคาลดลง จากก่อนประกาศใช้มาตรการ CL ยามีราคา 74.23 บาทต่อเม็ด ปัจจุบันมีราคาเหลือเพียง 13.21 บาทต่อเม็ด แม้ว่าสิทธิบัตรที่จดเพื่อคุ้มครองตัวยาโลพินาเวียร์และกระบวนการในการเตรียมได้หมดอายุไปแล้วตั้งแต่ปี 2559 ปัจจุบันยังมีคำขอสิทธิบัตรอย่างน้อย 1 ฉบับที่ยื่นขอคาไว้และอาจทำให้ยานี้ติดสิทธิบัตรจนถึงปี 2565 ถ้าไทยไม่ได้นำมาตรการ CL มาใช้ตั้งแต่ปี 2550 และยังมีผลบังคับใช้ในปัจจุบัน เป็นที่แน่นอนว่าราคายาโลพินาเวียร์/ลิโทนาเวียร์ที่เป็นยาต้นแบบที่บริษัทจดและยื่นจดสิทธิบัตรไว้ ยังจะมีราคาแพงมากจนประชาชนไม่สามารถเข้าถึงได้ และระบบหลักประกันสุขภาพฯ อาจไม่สามารถจ่ายยานี้ให้กับผู้ติดเชื้อเอชไอวีได้
2. ยาโอเซลทามิเวียร์ (Oseltamivir) มีการจดสิทธิบัตรในต่างประเทศก่อนที่ประเทศไทยจะเข้าเป็นสมาชิกในสนธิสัญญาความร่วมมือด้านสิทธิบัตรระหว่างประเทศ (PCT) ซึ่งไทยเป็นภาคี PCT ตั้งแต่ปี 2552 แต่ไม่มีการจดสิทธิบัตรในไทย ทำให้องค์การเภสัชกรรมสามารถผลิตได้ตั้งแต่ปี 2552 โดยเป็นยาหลักในการรักษาไข้หวัดใหญ่ ราคาในไทยก็ถูกกว่าราคาที่องค์กรสากลอย่าง UNICEF จัดซื้อให้ประเทศกำลังพัฒนาและประเทศพัฒนาน้อยโดยที่ยาโอเซลทามิเวียร์ขนาด 75 ม.ก. ที่ องค์การเภสัชกรรมมีราคาเม็ดละ 25 บาท ในขณะที่ราคาที่องค์กร UNICEF ซื้อได้มีราคาเม็ดละ 44.46 บาท ขณะนี้สิทธิบัตรในยาโอเซลทามิเวียร์ที่จดในสหรัฐฯ ส่วนใหญ่หมดอายุแล้ว
3. ในเรื่องคุณภาพของยาและมาตรฐานการผลิตยาทั้ง 2 ชนิด องค์การเภสัชกรรมใช้กระบวนการผลิตที่มีมาตรฐานการผลิตที่มีคุณภาพ โดยที่องค์การอนามัยโลก (World Health Organization) รับรองและเป็นที่ยอมรับของสากล มาตรฐานดังกล่าวเรียกว่า WHO-Pre Qualification เราจึงมั่นใจได้ว่ายาดังกล่าวมีคุณภาพ ประสิทธิผลและความปลอดภัย อีกทั้งยังสามารถจำหน่ายในราคาที่เหมาะสม ระบบหลักประกันสุขภาพทั้งสามระบบจึงสามารถจัดหายาที่มีคุณภาพและความปลอดภัยให้กับผู้ป่วยที่จำเป็นต้องใช้ โดยไม่มีปัญหาด้านงบประมาณ
ความท้าทายและข้อเสนอเกี่ยวกับระบบทรัพย์สินทางปัญญาเพื่อการเข้าถึงยา
1. การประกาศบังคับใช้สิทธิเพื่อผลิตหรือนำเข้ายาโดยรัฐ ตามมาตรา 51 ใน พ.ร.บ. สิทธิบัตร หรือที่เรียกว่า CL (Compulsory Licensing) นั้นเป็นมาตรการที่สอดคล้องตามความตกลงสากลว่าด้วยทรัพย์สินทางปัญญาขององค์การการค้าโลก ซึ่งเป็นมาตรการที่จำเป็นเพื่อแก้ไขการเข้าไม่ถึงยาในราคาไม่แพง เนื่องจากการผูกขาดด้วยระบบสิทธิบัตร และให้อำนาจรัฐใช้โดยไม่แสวงหากำไร
แต่กลไกนี้ตกเป็นเป้าหมายที่จะถูกกำจัดทิ้งเพราะเป็นอุปสรรคขัดขวางการทำกำไรของบรรษัทยาข้ามชาติ ความพยายามที่จะขจัดมาตรการ CL เช่นเดียวกับการขยายความคุ้มครองสิทธิบัตรให้มีอายุยาวนานมากกว่า 20 ปี การผูกขาดข้อมูลทางยา การบังคับใช้และตีความกฎหมายที่เกินเลย และการขัดขวางบริษัทยาชื่อสามัญด้วยกลไกต่างๆ กระทำผ่านการเจรจาความตกลงการค้าระหว่างประเทศฉบับต่างๆ เช่น เอฟทีเอระหว่างไทยและสหภาพยุโรป และระหว่างไทยกับสหรัฐฯ ที่เคยเจรจาและระงับการเจรจาไปชั่วคราว และในความตกลง CPTPP ที่เจรจาจบไปแล้วแต่ไทยต้องการเข้าร่วม
ความท้าทายจึงอยู่ที่การเจรจาเอฟทีเอฉบับต่างๆ ที่รัฐบาลต้องการจะรื้อฟื้นการเจรจา
เช่น เอฟทีเอไทย-สหภาพยุโรป หรือที่แม้แต่ต้องการลงนามในความตกลงที่สรุปไปแล้วโดยที่ไม่มีส่วนร่วมในการเจรจาเลย เช่น ความตกลง CPTPP โดยที่ไม่ได้คำนึงผลกระทบต่อการเข้าถึงยาและระบบหลักประกันสุขภาพฯ เท่าที่ควร ทั้งนี้ เมื่อลงนามในความตกลงเหล่านี้ไปแล้ว ไทยต้องแก้ไขกฎหมายต่างๆ ที่เกี่ยวข้อง รวมถึง พ.ร.บ. สิทธิบัตร ให้มีความเข้มงวดมากขึ้น ก่อให้เกิดการผูกขาดได้ง่ายและยาวนานมากขึ้น และจำกัดหรือขจัดการนำมาตรการ CL มาใช้
ความท้าทายจึงขึ้นอยู่กับความสามารถและความตระหนักของคณะเจรจาของไทย
ว่าจะสามารถเจรจาให้รักษากลไกนี้ให้ยังมีประสิทธิภาพได้อย่างในปัจจุบันหรือไม่ หรือจะถูกนำไปต่อรองแลกเปลี่ยนกับสิทธิพิเศษการค้าระยะสั้นเพื่อตัวเลขการส่งออก
ดังนั้น คณะเจรจาความตกลงการค้าจะต้องมีจุดยืนที่ชัดเจนและเข้มแข็ง ไม่นำเรื่องการเข้าถึงยาและระบบสาธารณสุขของประเทศไปต่อรอง
2. จากกรณีศึกษายาทั้งสองตัวนี้ เราจะเห็นได้ว่า การตรวจสอบคำขอสิทธิบัตรที่มีประสิทธิภาพและคุณภาพเป็นเรื่องสำคัญ เพราะในยาหนึ่งตัวบริษัทยาไม่ได้ยื่นขอรับสิทธิบัตรเพียงฉบับเดียว แต่บริษัทจะพลิกแพลงใช้ระบบสิทธิบัตรเอื้อประโยชน์ในตนเองให้ได้มากและนานที่สุด เพื่อคงสิทธิในการผูกขาดตลาด ทั้งในการผลิต การจำหน่าย การวิจัยไว้แต่เพียงผู้เดียวให้ได้นานที่สุด ซึ่งวิธีการแบบนี้เรียกว่า “สิทธิบัตรที่ยืดการผูกขาดให้ได้นานที่สุด” หรือ Evergreening
ถ้ากรมทรัพย์สินทางปัญญามีกระบวนการตรวจสอบคำขอรับสิทธิบัตรที่ไม่ดีพอ ผลที่จะเกิดขึ้น คือ ยาสำคัญๆ จะติดสิทธิบัตรไปอย่างยาวนาน และกีดขวางยาชื่อสามัญไม่ให้เข้าสู่ตลาดมาแข่งขัน สุดท้ายการผูกขาดดังกล่าวจะทำให้ยามีราคาแพงมากจนระบบหลักประกันสุขภาพของรัฐไม่สามารถจัดหาให้ผู้ป่วยเข้าถึงได้
ดังนั้นกรมทรัพย์สินทางปัญญาต้องพัฒนาคุณภาพการตรวจสอบสิทธิบัตรให้มีคุณภาพและประสิทธิภาพมากยิ่งขึ้นโดยเฉพาะการปฏิบัติตามคู่มือการตรวจสอบสิทธิบัตรทางเคมี
3. แม้ว่าสนธิสัญญา PCT (Patent Cooperation Treaty) ที่ไทยได้ลงนามเป็นแล้ว จะอำนวยความสะดวกในการยื่นขอรับสิทธิบัตรในส่วนที่เกี่ยวกับการเตรียมเอกสารในสามารถยื่นคำขอได้ในหลายๆ ประเทศในคราวเดียว แต่กลไกนี้ส่งผลให้ยื่นคำขอฯ ได้ง่ายขึ้นและทำให้จำนวนคำขอรับสิทธิบัตรเพิ่มขึ้นมาก รวมถึงภาระงานที่เจ้าหน้าที่ของกรมทรัพย์สินทางปัญญาจะเพิ่มมากขึ้น และจะส่งเสริมให้คุณภาพในการตรวจสอบที่ด้อยศักยภาพทวีความรุนแรงมากขึ้น
ดังนั้น กรมทรัพย์สินทางปัญญาจะต้องเพิ่มศักยภาพ และต้องไม่พิจารณาจากผลการพิจารณาในต่างประเทศโดยไม่พิจารณาในรายละเอียดคำขอ แต่ควรจะพิจารณาคำขอรับสิทธิบัตรด้วยความรอบคอบ โดยคำนึงถึงการพัฒนาอุตสาหกรรมผลิตยาในประเทศและการเข้าถึงยาด้วย
อีกทั้งยังต้องทำให้ฐานข้อมูลคำขอรับสิทธิบัตรและ สิทธิบัตรเข้าถึงได้ง่าย เป็นข้อมูลที่ทันสมัยตลอดเวลา ถูกต้อง และเข้าถึงได้อย่างทันท่วงทีเพื่อการตรวจสอบจากสาธารณะและป้องกันและลดการผูกขาดที่ไม่เป็นธรรม
4. พ.ร.บ. สิทธิบัตรฉบับปัจจุบันมีช่องโหว่ที่เอื้อให้เกิดการผูกขาดที่ไม่เป็นธรรม
โดยเฉพาะที่เกี่ยวข้องกับการเข้าถึงยา เช่น หลักเกณฑ์ในการพิจารณาสิทธิบัตรมีความคลุมเครือและให้อำนาจเจ้าหน้าที่ผู้ตรวจในการพิจารณา ระยะเวลาในการคัดค้านคำขอฯ สั้น ระยะเวลาที่จะเริ่มพิจารณาคำขอฯ นานในขณะที่การคุ้มครองเริ่มตั้งแต่วันที่ยื่นคำขอฯ มาตรการ CL ที่ยังไม่เอื้อให้มีการนำมาใช้ได้สะดวก เป็นต้น
กรมทรัพย์สินทางปัญญาได้ยกร่างแก้ไข พ.ร.บ. สิทธิบัตร และเปิดรับฟังความคิดเห็นผ่านทางออนไลน์ในช่วงรัฐประหารที่ผ่านมา ภาคประชาสังคม กลุ่มผู้ป่วยและนักวิชาการได้แสดงความคิดเห็นและเสนอให้แก้ไขร่างฯ ของกรมโดยให้มีมาตรการด้านทรัพย์สินทางปัญญาเพื่อส่งเสริมการเข้าถึงยา หรือที่เรียกว่ามาตรการยืดหยุ่นทริปส์เพื่อคุ้มครองการสาธารณสุข ให้มากขึ้นกว่าที่เป็นอยู่ แต่กรมฯ ไม่ได้นำความกังวลและข้อเสนอเหล่านั้นใส่ไว้ในร่างที่มีการแก้ไขล่าสุดก่อนยื่นให้กับสำนักงานคณะกรรมการกฤษฎีกา
แต่สิ่งสำคัญไปกว่านั้น กรมฯ ได้เสนอแก้ไขมาตราที่เกี่ยวกับมาตรการใช้สิทธิโดยรัฐ
หรือมาตรการ CL ซึ่งเป็นการกำจัดสิทธิของรัฐและก่อให้เกิดความยุ่งยากลหรือความกังวลแก่ผู้กำหนด นโยบายด้านสาธารณสุข ในอันที่จะนำมาตรการดังกล่าวมาใช้
โดยอนุญาตให้ผู้ทรงสิทธิ (ผู้ถือสิทธิบัตร) สามารถฟ้องร้องต่อศาลให้ยกเลิกมาตรการใช้สิทธิโดยรัฐที่หน่วยงานของรัฐประกาศใช้ไป
ทั้งนี้มาตรการดังกล่าวเป็นไปตามความตกลงระหว่างประเทศขององค์การการค้าโลก
และมีวัตถุประสงค์ที่จะปกป้องสาธารณะประโยชน์ของประเทศสมาชิกในเรื่องการเข้า
ถึงยาและสุขภาพ ดังนั้น กรมทรัพย์สินทางปัญญาควรนำเสนอร่าง พ.ร.บ. สิทธิบัตร
ที่แก้ไขหลังจากผ่านสำนักงานคณะกรรมการกฤษฎีกา มาเปิดรับฟังความคิดเห็นก่อนจะดำเนินการต่อ และควรนำข้อเสนอของภาคประชาสังคมที่เสนอไปในระหว่างการรับฟังความคิดเห็นผ่านออนไลน์ มาปรับแก้ไขในร่าง พ.ร.บ. สิทธิบัตรเพื่อขจัดปัญหาสิทธิบัตรที่ไม่มีคุณภาพและส่งเสริมการใช้มาตรการคุ้มครองสาธารณสุขให้มากยิ่งขึ้น
5. กลไกควบคุมราคายังไม่สามารถทำได้จริงและไม่มีประสิทธิภาพในปัจจุบัน ปัญหายามีสิทธิบัตรของไทยอย่างหนึ่ง คือ การไม่มีกลไกควบคุมราคายาที่จริงจัง แม้จะมี พ.ร.บ. ว่าด้วยราคาสินค้าและบริการ พ.ศ. 2542 ประกาศยาเป็นสินค้าควบคุมราคา แต่กระทรวงพาณิชย์ไม่มีมาตรการใดๆ ในการควบคุมราคายา ทำให้ยาที่มีสิทธิบัตรกำหนดราคายาได้อย่างตามใจชอบ ตัวอย่างที่เห็นชัดเจนคือยาต้านไวรัสเอชไอวีและยาต้านมะเร็งที่จนไทยต้องประกาศใช้มาตรการ CL
ดังนั้น กรมการค้าภายใน ภายใต้กระทรวงพาณิชย์ จำเป็นต้องนำ พ.ร.บ. ราคาสินค้าและบริการ พ.ศ. 2542 มาบังคับใช้อย่างจริงจังให้มากไปกว่าการกำหนดให้แสดงราคาที่บรรจุภัณฑ์และให้โรงพยาบาลแจ้งราคายา ให้ผู้ป่วยและญาติทราบเท่านั้น แต่ต้องดำเนินการให้ผู้ประกอบการแจ้งโครงสร้างราคายาและกำกับดูแลและควบคุมให้มีราคาที่เป็นธรรมต่อประชาชน
รายชื่อผู้แถลงข่าว
1. รศ.ดร.ภญ.จิราพร ลิ้มปานานนท์ นายกสภาเภสัชกรรม
2. รศ.ดร.ภญ.นุศราพร เกษสมบูรณ์ คณะเภสัชศาสตร์ มหาวิทยาลัยขอนแก่น
3. ผศ.ดร.ภญ.นิยดา เกียรติยิ่งอังศุลี ผู้จัดการศูนย์วิชาการเฝ้าระวังและพัฒนาระบบยา (กพย.)
4. เฉลิมศักดิ์ กิตติตระกูล มูลนิธิเข้าถึงเอดส์
5. น.ส.กรรณิการ์ กิจติเวชกุล FTA Watch

ร่วมบริจาคเงิน สนับสนุน ประชาไท โอนเงิน กรุงไทย 091-0-10432-8 "มูลนิธิสื่อเพื่อการศึกษาของชุมชน FCEM" หรือ โอนผ่าน PayPal / บัตรเครดิต (รายงานยอดบริจาคสนับสนุน)